تمام عملکردهای بیولوژیکی به نحوه تعامل پروتئینهای مختلف با یکدیگر بستگی دارد. تعاملات پروتئین-پروتئین همه چیز را از رونویسی DNA و کنترل تقسیم سلولی گرفته تا عملکردهای سطح بالاتر در موجودات پیچیده تسهیل میکند.
با این حال، هنوز مشخص نیست که چگونه این عملکردها در سطح مولکولی تنظیم میشوند و چگونه پروتئینها با یکدیگر تعامل میکنند - چه با پروتئینهای دیگر و چه با نسخههایی از خود.
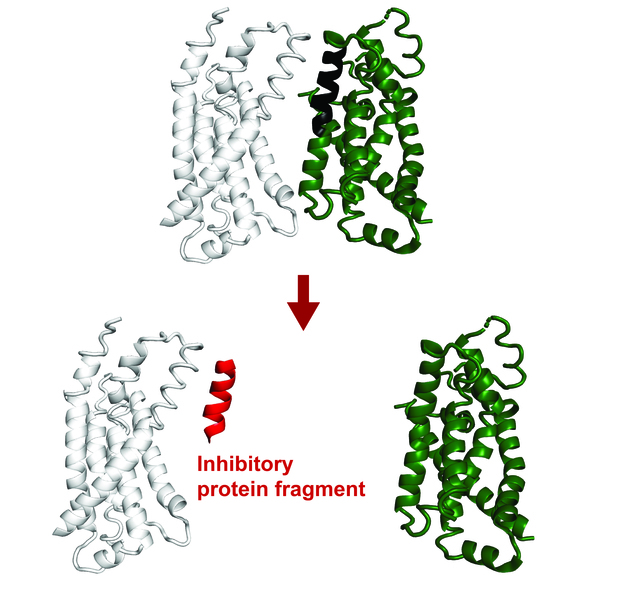
یافتههای اخیر نشان داده است که قطعات کوچک پروتئینی پتانسیل عملکردی زیادی دارند. حتی اگر قطعات ناقصی باشند، کشیدگیهای کوتاه اسیدهای آمینه همچنان میتوانند به رابطهای یک پروتئین هدف متصل شوند و تعاملات بومی را تکرار کنند. از طریق این فرآیند، آنها میتوانند عملکرد آن پروتئین را تغییر دهند یا تعاملات آن را با سایر پروتئینها مختل کنند.
بنابراین، قطعات پروتئینی میتوانند تحقیقات پایه در مورد تعاملات پروتئینی و فرآیندهای سلولی را تقویت کنند و به طور بالقوه کاربردهای درمانی داشته باشند.
اخیراً در مجموعه مقالات آکادمی ملی علوم منتشر شده است، روش جدیدی که در دپارتمان زیستشناسی توسعه یافته است، بر اساس مدلهای هوش مصنوعی موجود است تا به طور محاسباتی قطعات پروتئینی را پیشبینی کند که میتوانند به پروتئینهای کامل در E. coli متصل شده و آنها را مهار کنند. از لحاظ نظری، این ابزار میتواند منجر به مهارکنندههای ژنتیکی قابل رمزگذاری در برابر هر پروتئینی شود.
این کار در آزمایشگاه Gene-Wei Li، استادیار زیستشناسی و محقق موسسه پزشکی Howard Hughes، با همکاری آزمایشگاه Jay A. Stein (1968)، استاد زیستشناسی، استاد مهندسی زیستی و رئیس دپارتمان Amy Keating انجام شد.
بهرهگیری از یادگیری ماشین
این برنامه، به نام FragFold، از AlphaFold، یک مدل هوش مصنوعی که به دلیل توانایی آن در پیشبینی تاشدگی پروتئین و تعاملات پروتئین، منجر به پیشرفتهای چشمگیری در زیستشناسی در سالهای اخیر شده است، استفاده میکند.
هدف این پروژه پیشبینی مهارکنندههای قطعهای بود که یک کاربرد جدید از AlphaFold است. محققان در این پروژه به طور تجربی تأیید کردند که بیش از نیمی از پیشبینیهای FragFold برای اتصال یا مهار دقیق بودند، حتی زمانی که محققان هیچ داده ساختاری قبلی در مورد مکانیسمهای آن تعاملات نداشتند.
اندرو ساوینوف، نویسنده اول و مسئول این مقاله و محقق فوق دکترا در آزمایشگاه Li میگوید: «نتایج ما نشان میدهد که این یک رویکرد قابل تعمیم برای یافتن حالتهای اتصال است که احتمالاً عملکرد پروتئین را مهار میکنند، از جمله برای اهداف پروتئینی جدید، و میتوانید از این پیشبینیها به عنوان نقطه شروعی برای آزمایشهای بیشتر استفاده کنید.» «ما واقعاً میتوانیم این را برای پروتئینها بدون عملکردهای شناخته شده، بدون تعاملات شناخته شده، حتی بدون ساختارهای شناخته شده اعمال کنیم، و میتوانیم به این مدلهایی که در حال توسعه آن هستیم، اعتبار ببخشیم.»
یکی از این موارد FtsZ است، پروتئینی که برای تقسیم سلولی کلیدی است. این پروتئین به خوبی مطالعه شده است، اما حاوی ناحیهای است که ذاتاً نامنظم است و بنابراین، به ویژه مطالعه آن چالشبرانگیز است. پروتئینهای نامنظم پویا هستند و تعاملات عملکردی آنها بسیار زودگذر است - آنقدر کوتاه رخ میدهد که ابزارهای زیستشناسی ساختاری فعلی نمیتوانند یک ساختار یا تعامل واحد را ثبت کنند.
محققان از FragFold برای بررسی فعالیت قطعات FtsZ، از جمله قطعات ناحیه ذاتاً نامنظم، برای شناسایی چندین تعامل اتصال جدید با پروتئینهای مختلف استفاده کردند. این جهش در درک، آزمایشهای قبلی اندازهگیری فعالیت بیولوژیکی FtsZ را تأیید و گسترش میدهد.
این پیشرفت تا حدی به این دلیل قابل توجه است که بدون حل ساختار ناحیه نامنظم انجام شده است و به این دلیل که پتانسیل قدرت FragFold را نشان میدهد.
Keating میگوید: «این یک نمونه از این است که چگونه AlphaFold اساساً نحوه مطالعه زیستشناسی مولکولی و سلولی را تغییر میدهد.» «کاربردهای خلاقانه روشهای هوش مصنوعی، مانند کار ما در FragFold، قابلیتهای غیرمنتظره و مسیرهای تحقیقاتی جدیدی را باز میکنند.»
مهار، و فراتر از آن
محققان این پیشبینیها را با قطعهقطعه کردن محاسباتی هر پروتئین و سپس مدلسازی نحوه اتصال آن قطعات به شرکای تعاملی که فکر میکردند مرتبط هستند، انجام دادند.
آنها نقشههای اتصال پیشبینیشده را در سراسر توالی کامل با اثرات همان قطعات در سلولهای زنده مقایسه کردند، که با استفاده از اندازهگیریهای تجربی با توان بالا تعیین شد که در آن میلیونها سلول هر کدام یک نوع قطعه پروتئینی تولید میکنند.
AlphaFold از اطلاعات همتکاملی برای پیشبینی تاشدگی استفاده میکند و معمولاً تاریخچه تکاملی پروتئینها را با استفاده از چیزی به نام همترازی توالیهای چندگانه برای هر بار اجرای پیشبینی ارزیابی میکند. MSAها حیاتی هستند، اما یک گلوگاه برای پیشبینیهای در مقیاس بزرگ هستند - آنها میتوانند مقدار زیادی زمان و قدرت محاسباتی را صرف کنند.
برای FragFold، محققان در عوض MSA را برای یک پروتئین کامل یک بار از قبل محاسبه کردند و از آن نتیجه برای هدایت پیشبینیها برای هر قطعه از آن پروتئین کامل استفاده کردند.
Savinov، به همراه Sebastian Swanson فارغالتحصیل آزمایشگاه Keating، قطعات مهاری مجموعهای متنوع از پروتئینها را علاوه بر FtsZ پیشبینی کرد. از جمله تعاملاتی که آنها بررسی کردند، مجموعهای بین پروتئینهای انتقال لیپوپلی ساکارید LptF و LptG بود. یک قطعه پروتئینی LptG این تعامل را مهار کرد و احتمالاً تحویل لیپوپلی ساکارید را مختل کرد، که یک جزء حیاتی از غشای خارجی سلولی E. coli است که برای تناسب اندام سلولی ضروری است.
Savinov میگوید: «بزرگترین شگفتی این بود که ما میتوانیم اتصال را با چنین دقت بالایی پیشبینی کنیم و در واقع، اغلب اتصالی را پیشبینی میکنیم که مربوط به مهار است.» «برای هر پروتئینی که بررسی کردهایم، توانستهایم مهارکنندهها را پیدا کنیم.»
محققان در ابتدا بر قطعات پروتئینی به عنوان مهارکننده تمرکز کردند، زیرا اینکه آیا یک قطعه میتواند عملکرد ضروری در سلولها را مسدود کند یا خیر، یک نتیجه نسبتاً ساده برای اندازهگیری سیستماتیک است. ساوینوف همچنین مشتاق است که عملکرد قطعات را خارج از مهار، مانند قطعاتی که میتوانند پروتئینی را که به آن متصل میشوند تثبیت کنند، عملکرد آن را افزایش یا تغییر دهند، یا تخریب پروتئین را تحریک کنند، بررسی کند.
طراحی، در اصل
این تحقیق نقطه شروعی برای توسعه درک سیستماتیک از اصول طراحی سلولی و اینکه مدلهای یادگیری عمیق ممکن است از چه عناصری برای ارائه پیشبینیهای دقیق استفاده کنند، است.
Savinov میگوید: «یک هدف گستردهتر و دورتر وجود دارد که ما در حال ساختن آن هستیم.» «اکنون که میتوانیم آنها را پیشبینی کنیم، آیا میتوانیم از دادههایی که از پیشبینیها و آزمایشها داریم برای بیرون کشیدن ویژگیهای برجسته استفاده کنیم تا بفهمیم AlphaFold در واقع چه چیزی در مورد اینکه چه چیزی یک مهارکننده خوب میسازد، آموخته است؟»
Savinov و همکاران همچنین به بررسی بیشتر نحوه اتصال قطعات پروتئینی پرداختند، سایر تعاملات پروتئینی را بررسی کردند و با جهش دادن باقیماندههای خاص بررسی کردند که چگونه آن تعاملات نحوه تعامل قطعه با هدف خود را تغییر میدهند.
بررسی تجربی رفتار هزاران قطعه جهشیافته در داخل سلولها، رویکردی که به عنوان اسکن جهش عمیق شناخته میشود، اسیدهای آمینه کلیدی را نشان داد که مسئول مهار هستند. در برخی موارد، قطعات جهشیافته حتی مهارکنندههای قویتری نسبت به توالیهای طبیعی و کامل خود بودند.
سوانسون میگوید: «برخلاف روشهای قبلی، ما محدود به شناسایی قطعات در دادههای ساختاری تجربی نیستیم.» «نقطه قوت اصلی این کار، تعامل بین دادههای مهار تجربی با توان بالا و مدلهای ساختاری پیشبینیشده است: دادههای تجربی ما را به سمت قطعاتی که بهویژه جالب هستند، هدایت میکنند، در حالی که مدلهای ساختاری پیشبینیشده توسط FragFold یک فرضیه خاص و قابل آزمایش برای نحوه عملکرد قطعات در سطح مولکولی ارائه میدهند.»
Savinov در مورد آینده این رویکرد و کاربردهای بیشمار آن هیجانزده است.
Li موافق است: «FragFold با ایجاد بایندرهای فشرده و قابل رمزگذاری ژنتیکی، طیف گستردهای از امکانات را برای دستکاری عملکرد پروتئین باز میکند.» «ما میتوانیم قطعات عملکردی را که میتوانند پروتئینهای بومی را اصلاح کنند، محل زیرسلولی آنها را تغییر دهند و حتی آنها را برای ایجاد ابزارهای جدید برای مطالعه زیستشناسی سلولی و درمان بیماریها برنامهریزی مجدد کنند، تصور کنیم.»